GIỚI THIỆU CÁCH CHUẨN ĐỘ AXIT – BAZƠ
**PHƯƠNG PHÁP CHUẨN ĐỘ AXIT – BAZƠ** [Click để tham khảo các thiết bị chuẩn độ tại đây][1] 1. ** Đặc điểm.** - Dùng phương pháp này để xác định nồng độ
Nội dung
PHƯƠNG PHÁP CHUẨN ĐỘ AXIT – BAZƠ
Click để tham khảo các thiết bị chuẩn độ tại đây
- Đặc điểm.
- Dùng phương pháp này để xác định nồng độ axit, bazơ.
- Là phương pháp phân tích thể tích dựa trên phản ứng chuẩn độ:
H+ + OH- ¾® H2O
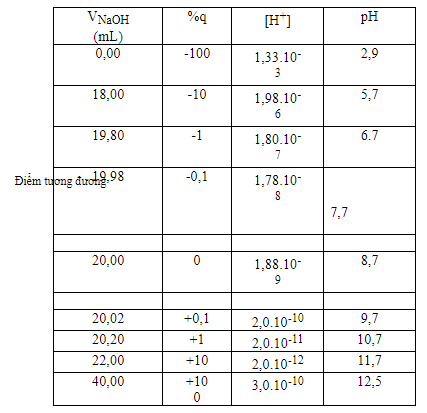
- Trong quá trình chuẩn độ nồng độ ion H+ và ion OH- luôn thay đổi nghĩa là pH dung dịch thay đổi.
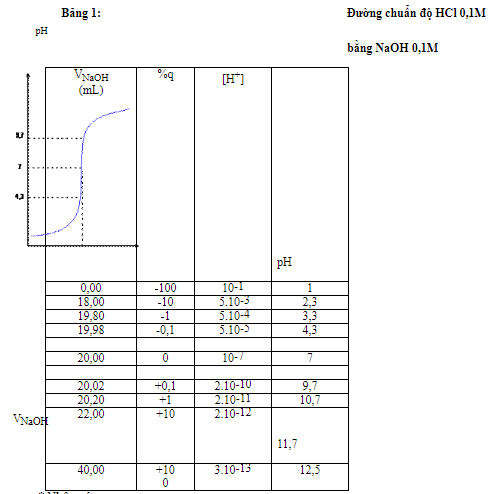
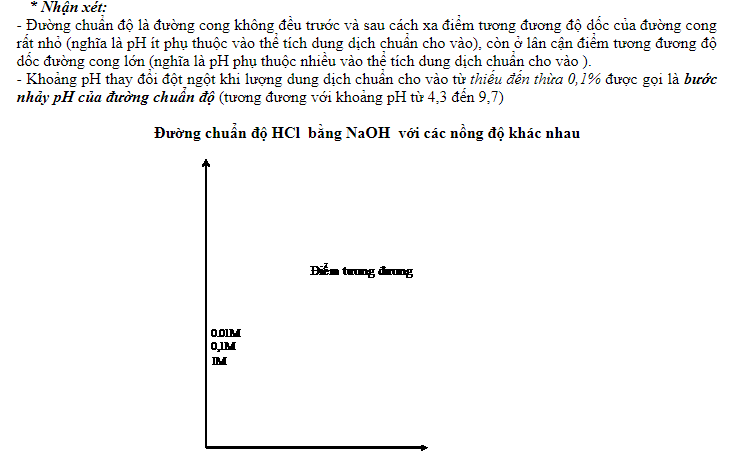
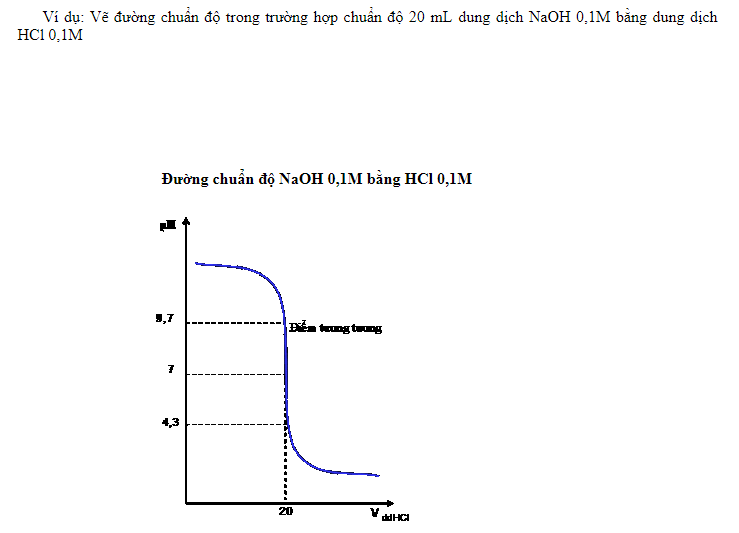
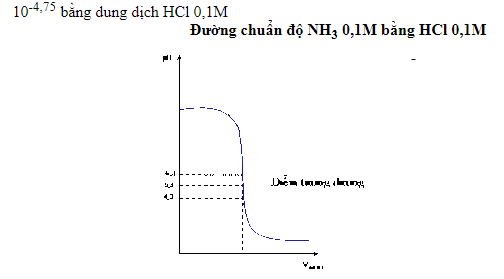
- Đường biểu diễn sự biến thiên của pH với lượng dung dịch chuẩn cho vào gọi là đường chuẩn độ axit – bazơ.
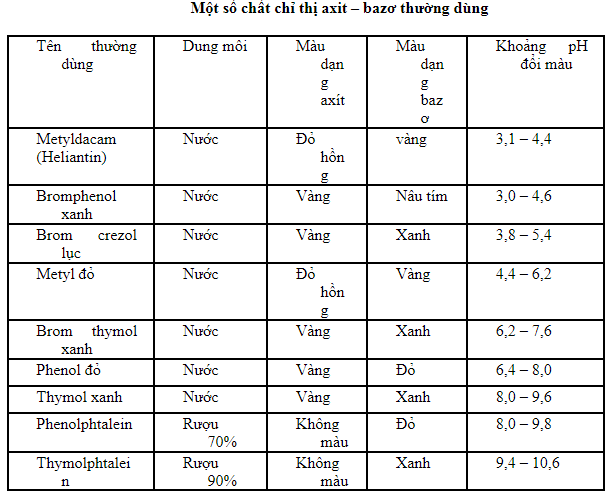
- Để xác định điểm tương đương trong quá trình chuẩn độ, người ta dùng chất chỉ thị axit – bazơ.
- Chất chỉ thị axit-bazơ (chất chỉ thị pH).
- Là những chất có màu thay đổi theo sự thay đổi của pH.
- Thường là những axit yếu hữu cơ (HInd) hoặc bazơ yếu hữu cơ (IndOH), trong đó, dạng axit (HInd; Ind+) và bazơ liên hợp (Ind-; IndOH) có màu khác nhau.
- Trong dung dịch chất chỉ thị tồn tại đồng thời 2 dạng axít và bazơ liên hợp có màu khác nhau:
HInd H+ + Ind- (a)
IndOH Ind+ + OH- (b)
- Nếu nồng độ của chúng hơn kém nhau không quá 10 lần Þ mắt ta thấy sự tồn tại của cả 2 dạng màu.
- Nếu nồng độ của chúng hơn nhau từ 10 lần trở lên, mắt ta nhìn thấy màu của dạng có nồng độ lớn hơn.
Ví dụ: chỉ thị metyldacam là axit yếu (HInd) trong dung dịch tồn tại cân bằng phân ly
HInd H+ + Ind-
Đỏ Vàng









Máy chuẩn độ Hanna Click xem chi tiết

Nguồn: Sưu tầm
